 当前位置:首页 > 研究领域 > 神经系统
当前位置:首页 > 研究领域 > 神经系统
记忆印迹是否以及如何在细胞集群水平上组织一直是神经科学中的一个基本问题。学习信息的编码如何实现,以及记忆的灵活性又是如何通过细胞集群构成的印迹来支持,仍然难以捉摸。近期,清华大学钟毅教授团队在Neuron (IF 15) 上发表文章“Identification of an engram ensemble mediating memory forgetting in the dentate gyrus”,提出了一种新的记忆模型,该模型由小鼠齿状回中两个正交的、被学习招募的神经元集群编码:Fos 集群编码记忆,而 NRAM 集群则编码遗忘。这一发现为理解记忆灵活性如何实现提供了新的见解。

| 实验动物 | 7月龄野生型小鼠和AD小鼠 |
|---|---|
| 病毒产品 |
AAV2/9-NRAM-d2tTA AAV2/9-Fos-tTA AAV2/9-Fos-ERT2CreERT2-PEST |
| 注射方式 | 定位注射 |
| 注射剂量 | 100nL |
| 注射部位 | 背侧齿状回dDG |
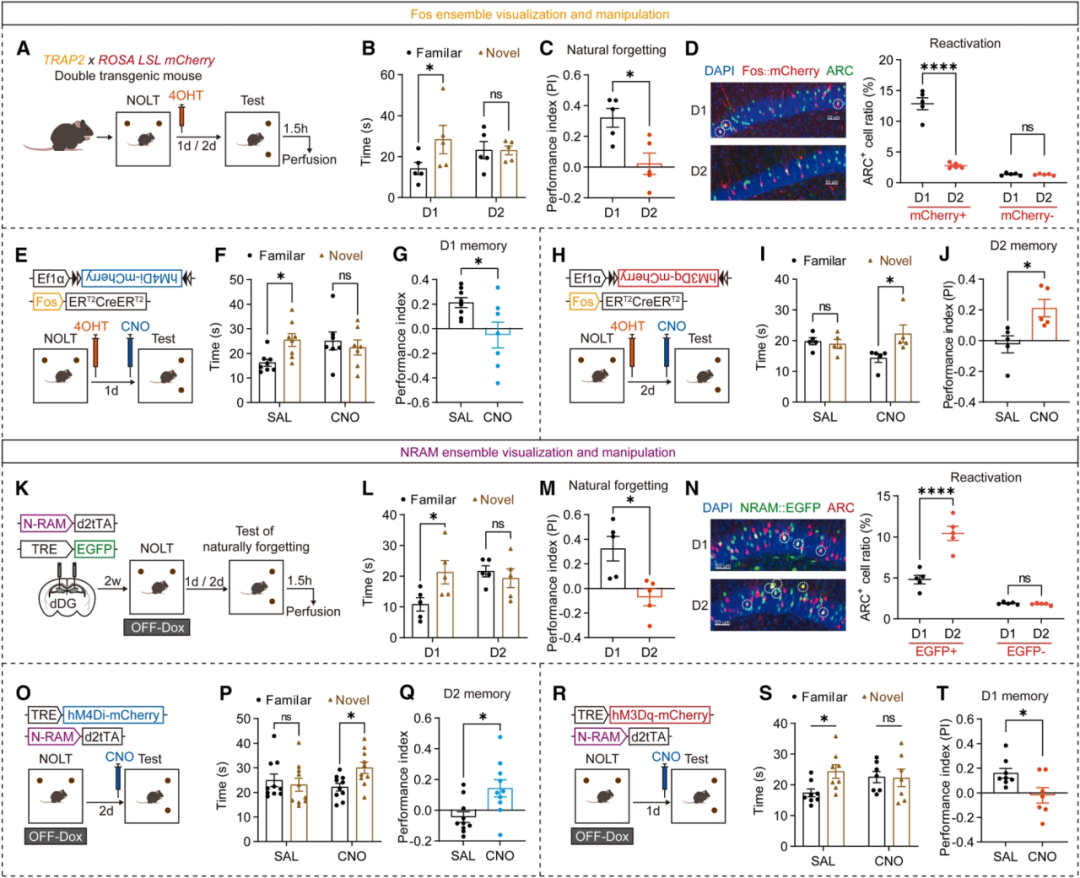
作者发现单电击情景恐惧记忆的提取是由记忆和遗忘集群的活动决定的:刺激Fos集群或抑制NRAM集群会导致遗忘减少,而反向操纵则会引发遗忘。作者进一步在新物体定位(NOL)任务中探究了记忆提取的调控机制。发现第1天NOL测试中,小鼠花更多时间探索移动的物体,但这种偏好在第2天消失了,同时Fos集群的再激活率从第1天到第2天显著下降,反映出NOL记忆的自然遗忘将Fos集群切换到沉默状态。化学遗传学抑制Fos集群阻止了训练后第1天NOL记忆的提取,而激活则恢复第2天NOL记忆的提取。此外随着记忆自然衰退,第2天NOL测试期间的NRAM集群再激活率明显高于第1天,化学遗传学抑制NRAM集群恢复了遗忘的NOL记忆,但激活引起了NOL记忆损伤,表明NRAM整体的活动促进了NOL记忆遗忘。这些结果表明Fos集群驱动记忆表达,NRAM集群驱动遗忘表达,更重要的是,通过操纵任一集群激活或抑制,可能会影响记忆。
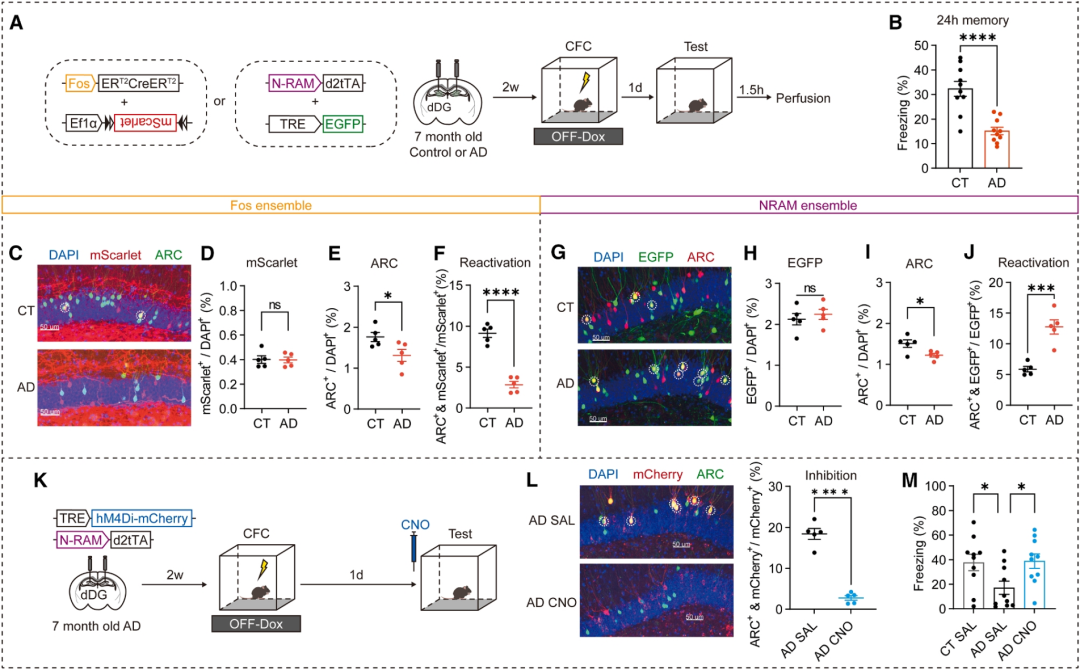
已有研究表明早期阿尔茨海默病(AD)小鼠模型中存在沉默的Fos集群体和Rac1依赖性的加速遗忘。作者在在早期AD小鼠模型中检查了回忆诱导的记忆激活和遗忘。发现AD小鼠在一次电击CFC后24小时表现出记忆障碍,尽管WT和AD小鼠之间的Fos集群标记相当,但在回忆过程中AD小鼠的Fos集群再激活显著减少,AD小鼠的NRAM集群激活高于WT小鼠。作者进一步测试回忆过程中NRAM集群过度活跃而导致AD小鼠遗忘症的可能性,发现NRAM集群的化学遗传学抑制成功地挽救了早期AD小鼠的记忆障碍,这表明NRAM集群的过度活跃是观察到的遗忘症的基础。
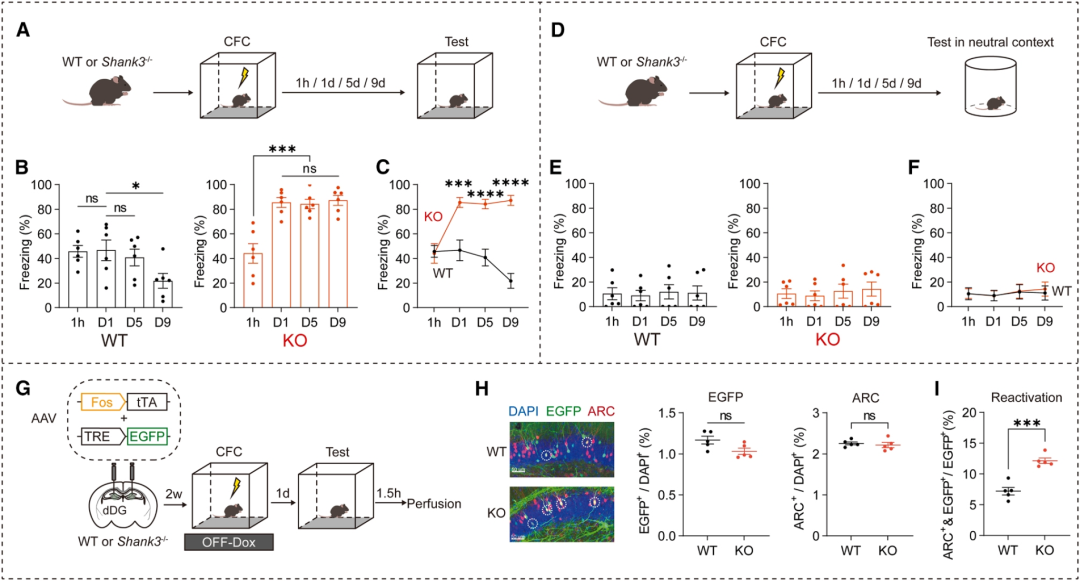
已有研究发现,多个自闭症风险基因的突变果蝇会出现遗忘缺陷,这促使作者测试自闭症小鼠模型中NRAM集群介导的遗忘是否受到破坏。Shank3是自闭症候选基因之一,作者比较了WT和Shank3敲除(KO)小鼠之间的单次电击恐惧记忆表型,发现Shank3 KO小鼠的第1天记忆显著增强;随着时间的推移,WT小鼠的记忆开始随着时间的推移而衰退,而Shank3 KO小鼠没有表现出明显的衰退并保持较高的记忆水平。接下来,作者检查了WT和Shank3 KO小鼠中Fos整体的重新激活情况,发现KO小鼠在第1天回忆时的再激活水平显著高于WT小鼠。这些结果表明,在Shank3 KO小鼠中,由NRAM集群介导的遗忘机制被破坏。
本研究提出了一种新颖的记忆印迹模型,由小鼠齿状回中两个正交学习招募的神经元集合编码:Fos集群编码记忆,NRAM集群编码遗忘。在阿尔茨海默病和自闭症小鼠模型中观察到的记忆异常主要与遗忘整体的功能障碍有关,表明遗忘背后的机制是认知障碍的关键靶点。
备案号:鲁ICP备13011878号 网址:www.wzbio.com.cn









