 当前位置:首页 > 研究领域 > 其他
当前位置:首页 > 研究领域 > 其他
文章标题:Inhibition of tubular epithelial cells ferroptosis alleviates renal interstitial fibrosis by reducing lipid hydroperoxides and TGF-β/Smad signaling
发表期刊:Cell Communication and Signaling (IF 8.9)
合作客户:华中科技大学同济医学院附属同济医院高红宇/颜奇研究团队
| 基因信息 | GPX4:谷胱甘肽过氧化物酶 4 |
|---|---|
| 实验动物 | 8周龄C57BL/6小鼠 |
| 病毒产品 |
AAV9-mGPX4 、AAV9-vector |
| 病毒用量 | 2.0×1010pfu |
| 注射方式 | 肾实质内注射 |
肾脏疾病是现代社会的主要健康问题,肾纤维化是慢性肾脏病(CKD)的最终共同途径,但目前治疗手段有限。铁死亡作为一种非凋亡形式的调节性细胞死亡,参与多种疾病进程,在CKD中铁过载可导致肾损伤和纤维化,抑制铁死亡可能是缓解肾纤维化的有效策略。谷胱甘肽过氧化物酶4(GPX4)是铁死亡的关键调节因子,但其在纤维化肾脏中影响铁死亡的具体机制尚不清楚。
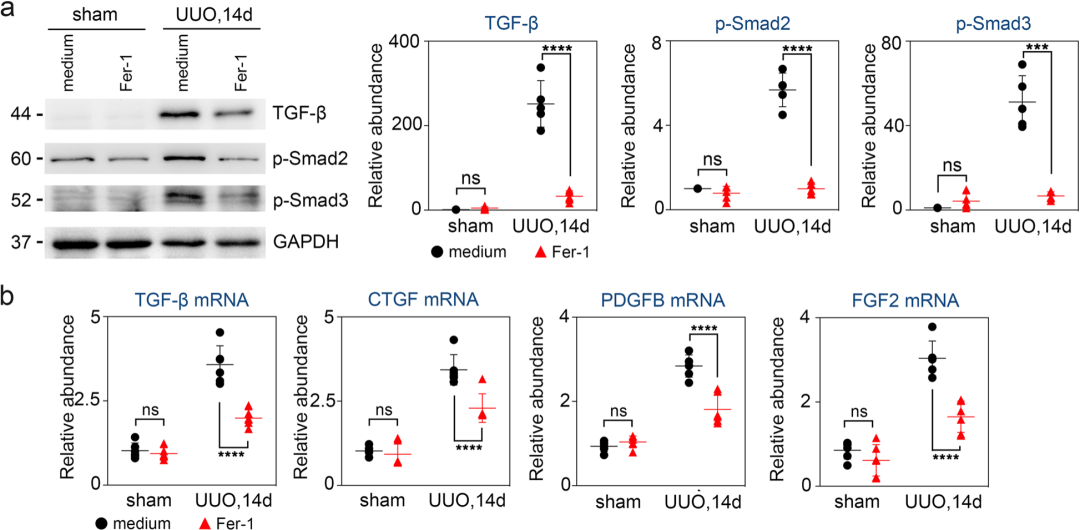
通过构建单侧输尿管梗阻(UUO)小鼠模型,研究发现铁死亡在肾小管上皮细胞(TECs)中持续发生,且与肾间质纤维化进程密切相关;对UUO小鼠使用铁死亡抑制剂Fer-1,结果表明抑制铁死亡能有效缓解肾纤维化。此外,Fer-1处理后,梗阻肾脏中TGF-β及其关键下游效应物p-Smad2、p-Smad3,以及CTGF、PDGFB、FGF2的水平显著降低,表明Fer-1通过抑制TGF-β/Smad信号通路,减少促纤维化细胞因子的释放,进而减轻肾间质纤维化。体外实验进一步验证Fer-1能有效改善TGF-β诱导的HK-2细胞铁死亡积累并缓解细胞纤维化。上述结果证实铁死亡在肾纤维化过程中起着关键作用,它通过持续激活 TGF-β/Smad信号通路,促进下游促纤维化因子的释放,最终导致纤维化的发生,而抑制铁死亡可以有效减轻TGF-β诱导的纤维化反应。
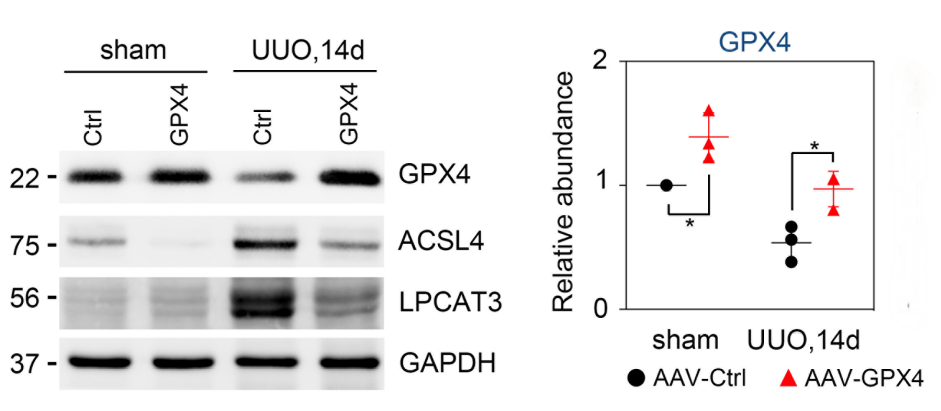
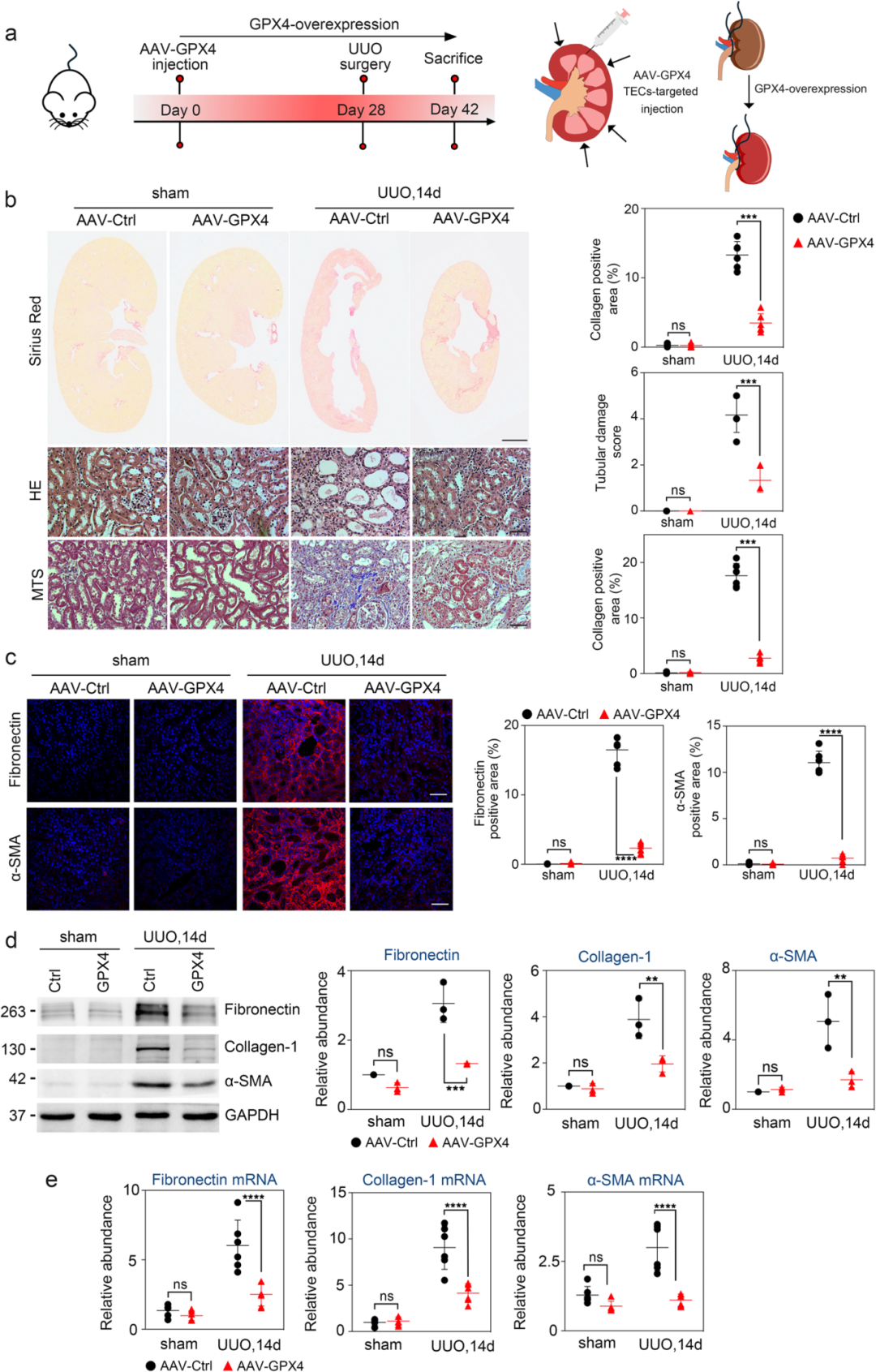
为进一步明确TEC铁死亡在肾间质纤维化中的作用,研究团队采用AAV载体将mGPX4导入小鼠肾脏近端TECs,成功实现GPX4在小鼠肾脏组织中的有效过表达。在 UUO 14 天后,注射AAV9-Vector的对照组小鼠出现GPX4 表达下降、脂质氢过氧化物(4-HNE)积累以及TUNEL阳性细胞增多的现象;而在GPX4过表达小鼠中,这些铁死亡相关的变化被显著抑制。同时,脂质代谢酶ACSL4和LPCAT3在GPX4过表达小鼠中也有效降低。这表明在 UUO 过程中,过表达 GPX4 能够有效修复 TECs 的铁死亡,逆转铁死亡的进展。对UUO诱导的小鼠肾脏进行观察,发现其出现严重的形态学病变,如肾小管扩张、肾小管间质扩张以及间质胶原沉积,而 GPX4 过表达(GPX4-OE)的小鼠肾脏形态学异常明显减少,表明GPX4过表达减轻肾脏的病理损伤。免疫荧光分析发现 GPX4-OE 显著抑制纤维化标志物表达水平,这些实验结果证明GPX4过表达保护TEC免受铁死亡,减轻肾间质纤维化。进一步分析发现抑制TEC铁死亡可通过抑制TGF-β/Smad信号通路,对肾间质纤维化起到保护作用。
本研究揭示肾小管上皮细胞铁死亡是肾纤维化疾病的关键病理机制,抑制TECs铁死亡可有效改善肾间质纤维化,显著降低促纤维化因子的表达,其作用机制与抑制TGF-β/Smad信号通路有关。这表明抑制TECs铁死亡可能是预防和治疗CKD的一种有前景的策略。
备案号:鲁ICP备13011878号 网址:www.wzbio.com.cn









