【维真细胞系】案例1:原位CAR细胞疗法
靶向 CD47-SIRPα 轴具有巨大的治疗潜力,但其临床转化却因剂量限制性血液毒性和治疗药物的瘤内递送效率低下而受阻。上海交通大学研究团队开发了一套整合式生物工程平台,可同时解决这两大难题。研究人员设计了一种基于仿生 SIRPα 的嵌合抗原受体(CAR),该受体通过亲和力驱动机制发挥作用,能在功能上区分肿瘤细胞表面的高密度 CD47 表达与红细胞表面的低密度 CD47 分布。将编码该受体的信使核糖核酸(mRNA)通过肽功能化脂质纳米颗粒(LNP) 进行瘤内递送时,该系统可实现对肿瘤相关巨噬细胞(CAR-TAM)的选择性、空间限制性重编程。本研究为原位细胞免疫治疗构建了一套安全、可转化的技术方案,为解决靶向泛表达抗原的核心难题提供了综合性解决方案。
靶向 CD47-SIRPα 轴具有巨大的治疗潜力,但其临床转化却因剂量限制性血液毒性和治疗药物的瘤内递送效率低下而受阻。上海交通大学研究团队开发了一套整合式生物工程平台,可同时解决这两大难题。研究人员设计了一种基于仿生 SIRPα 的嵌合抗原受体(CAR),该受体通过亲和力驱动机制发挥作用,能在功能上区分肿瘤细胞表面的高密度 CD47 表达与红细胞表面的低密度 CD47 分布。将编码该受体的信使核糖核酸(mRNA)通过肽功能化脂质纳米颗粒(LNP) 进行瘤内递送时,该系统可实现对肿瘤相关巨噬细胞(CAR-TAM)的选择性、空间限制性重编程。本研究为原位细胞免疫治疗构建了一套安全、可转化的技术方案,为解决靶向泛表达抗原的核心难题提供了综合性解决方案。
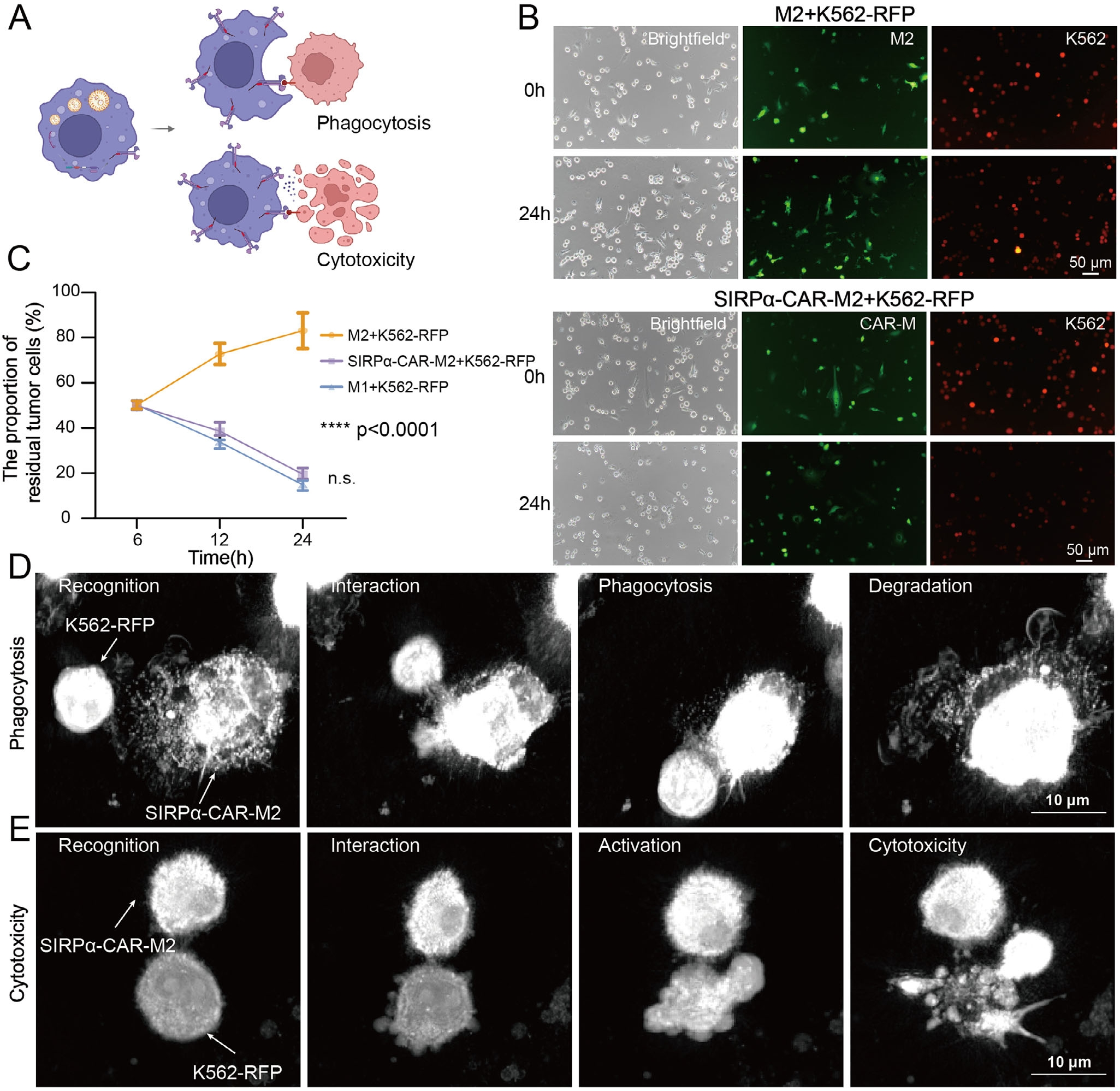
经改造的SIRPα-CAR巨噬细胞具备双重抗肿瘤机制,并发生强效促炎性重编程
|
【维真细胞系】案例2:银屑病
中心体是调控微管组织与细胞有丝分裂进程最重要的无膜细胞器之一。卷曲螺旋α-螺旋杆蛋白1(CCHCR1,亦称 HCR) 基因被认为是银屑病易感基因,且该蛋白在哺乳动物细胞中定位于P小体与中心体。然而,HCR的确切细胞功能及其在中心体中潜在的调控作用仍未被阐明。深圳大学、汕头大学医学院研究团队联合阐明HCR在中心体中的核心功能:HCR 通过C端卷曲螺旋结构域与中心体蛋白astrin直接结合,被astrin招募至中心体并免受泛素-蛋白酶体降解;HCR进一步招募CEP72 及小头畸形相关蛋白(CEP152、CEP63、CDK5RAP2) 至中心体,调控中心粒复制、微管组装与有丝分裂正常进行;敲除HCR会引发多极纺锤体、基因组不稳定、DNA 损伤及肿瘤增殖能力下降,证实HCR与astrin协同维持中心体功能与基因组稳定性。
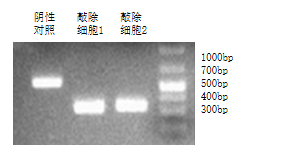
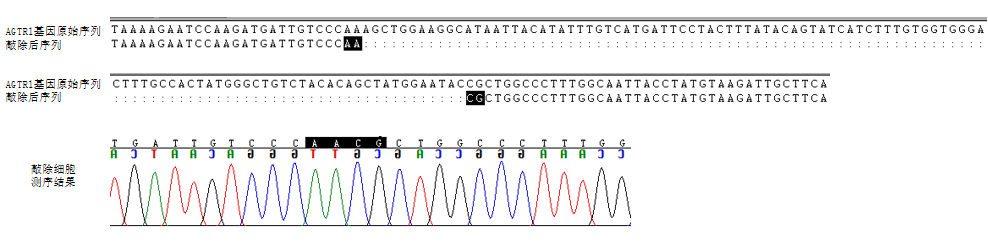
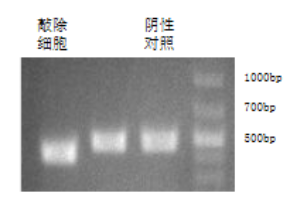
利用CRISPR/Cas9构建HCR敲除HeLa细胞系(HCR-KO),证实HCR缺失导致 CEP72无法定位到中心体、细胞周期M期阻滞、体外克隆形成能力下降以及体内成瘤能力显著降低。
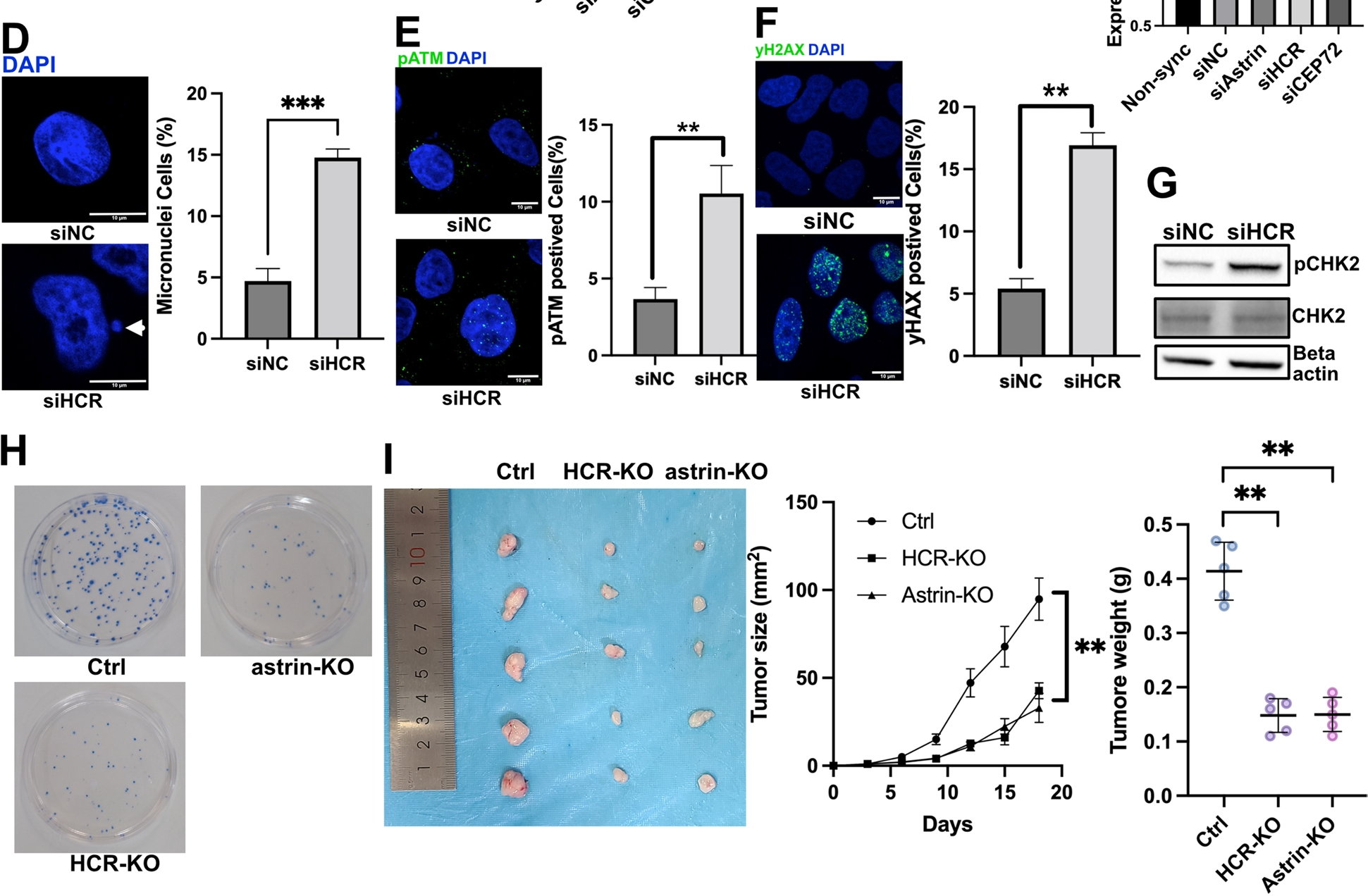
HCR缺失导致有丝分裂缺陷、DNA损伤和肿瘤增殖降低
|
【维真细胞系】案例3:免疫细胞互作机制
先天性淋巴细胞(ILCs)是先天免疫系统中与辅助性T细胞相对应的细胞群体,与辅助性T细胞共享多种表型特征。可诱导T细胞共刺激分子(ICOS)在T细胞上表达,参与T细胞活化以及淋巴组织中T细胞与B细胞之间的相互作用。然而,ICOS在ILC3s以及ILC3s与免疫微环境相互作用中的角色仍不明确。吉林大学第一医院研究团队发现,人ILC3s上ICOS的表达与其活化状态相关。ICOS共刺激能够增强ILC3s的存活、增殖以及产生细胞因子(IL-22、IL-17A、IFN-γ、TNF和GM-CSF)的能力。通过ICOS与CD40信号的协同效应,B细胞促进了ILC3s的功能,而ILC3s诱导的、不依赖T细胞的B细胞IgA和IgM分泌主要依赖于CD40信号通路。因此,ICOS对于ILC3s发挥其不可替代的作用以及ILC3s与邻近B细胞之间的相互作用至关重要。
为了验证ICOSL对ILC3的直接共刺激作用,将CD32/ICOSL过表达细胞系以及CD32空载体细胞系分别与人扁桃体 ILC3 共培养,检测细胞因子。结果显示高表达ICOSL的细胞可以直接激活ILC3,显著提升 IL-22、IL-17A、IFN-γ、TNF、GM-CSF分泌。
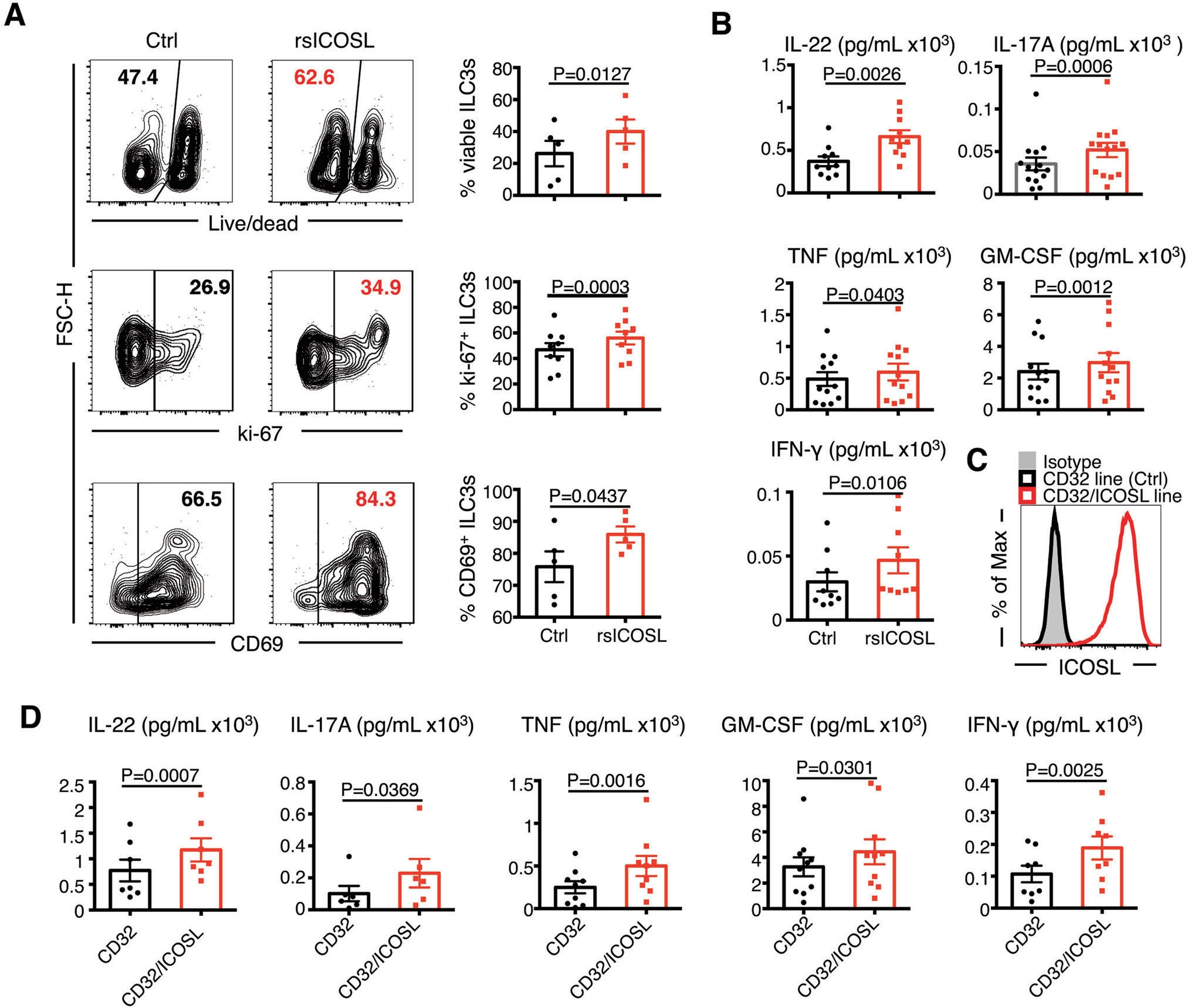
ICOS共刺激增强ILC3的存活、增殖和活化
|
【维真细胞系】案例4:肾脏衰老及纤维化
急性肾损伤(AKI)可进展为慢性肾脏病(CKD),这一转变由细胞衰老(一种不可逆的细胞周期停滞状态)所驱动。然而,促进这一病理过程的分子机制尚不明确。南方医科大学南方医院研究团队发现,通道蛋白Pannexin1(Panx1)会促进这种有害的衰老以及随后发生的肾脏纤维化。研究揭示,Panx1在内质网(细胞内的关键钙离子储存库)中发挥非经典功能,即作为钙离子泄漏通道,这种Panx1介导的钙泄漏发生在线粒体与内质网的接触位点,导致线粒体钙超载、功能障碍以及促衰老信号的产生。在雄性小鼠AKI模型中,基因敲除Panx1可减轻肾脏衰老与纤维化。确定了定位于内质网的Panx1是肾脏疾病进展的关键驱动因子,并是一个潜在的治疗靶点。
利用CRISPR-Cas9构建Panx1敲除的HK-2细胞系,在Panx1-KO HK-2中转染内质网定位截短体Panx11-89,证明仅内质网Panx1就足以驱动细胞衰老,是Panx1促衰老的功能位点。
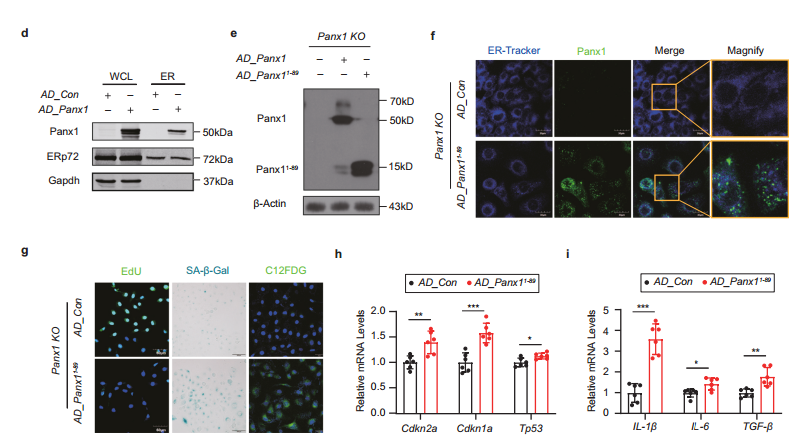
ER定位的Panx1上调诱导细胞衰老
|